Клинические исследования в России: какие шаги делает большая фарма?

В связи со сложившейся политической ситуацией некоторые фармацевтические компании объявили об ограничениях работы в России, однако радикальных заявлений об уходе с российского рынка пока не прозвучало. Но даже заявленные ограничения повлияют на портфель разработок этих компаний, что затронет фармацевтический сектор в целом и может привести к задержке выхода новых лекарств во всём мире. Представляем аналитику pharmaceutical-technology.com.
Из ТОП-10 глобальных фармацевтических производителей, проводящих крупные многоцентровые клинические исследования с участием российских клинических центров, Bristol Myers Squibb (BMS), GlaxoSmithKline (GSK), Johnson&Johnson, Merck, Novartis, Novo Nordisk, Pfizer и Roche отметили, что они прекратили регистрацию новых пациентов-участников. BMS, GSK, Novartis, Novo Nordisk и Pfizer также заявили о приостановке новых исследований в России. Roche добавила, что не будет инициировать создание новых исследовательских центров.
Представитель «AstraZeneca» сообщил Clinical Trials Arena, что компания приостановила регистрацию новых пациентов в уже начатые КИ и в настоящее время не начинает никаких новых клинических испытаний. У компании также нет планов по новым инвестициям в Россию. Sanofi продолжает текущие испытания с участием российских пациентов, но приостановила все расходы, не связанные с поставкой жизненно важных лекарств и вакцин. (Топ-10 основан на базе данных клинических испытаний GlobalData).
Значительное количество клинических исследований в фазах
I–III, спонсируемые крупными фармацевтическими компаниями с площадками в
России, всё ещё набирают участников испытаний.
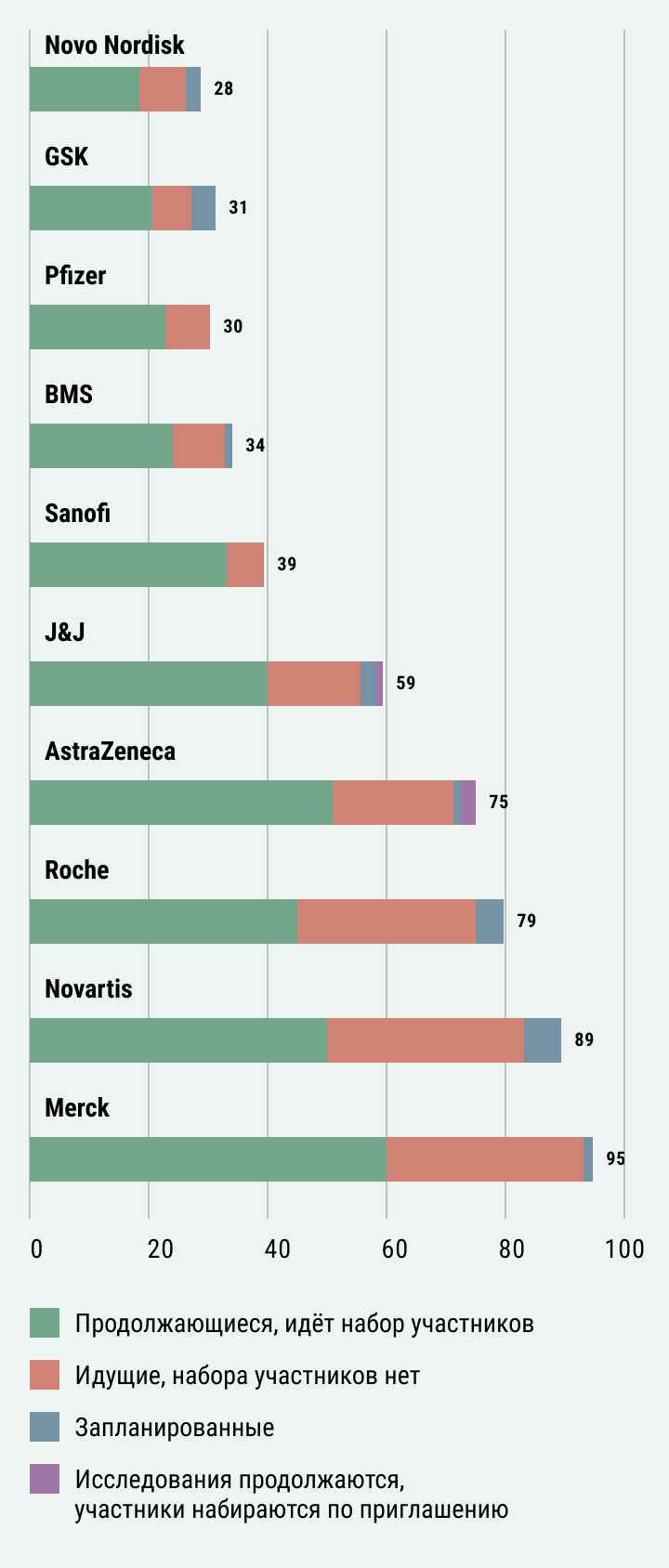
Причины, по которым компании продолжают или прекращают клинические исследования в России, могут различаться. Часть уходящих компаний заявили о несогласии с политическим курсом, другие о сложностях в поддержании связей, вызванных новыми экономическими санкциями. Об этом, в частности, сказала Дана Лефф Недзельска, соучредитель и генеральный директор CRO August Research. «Кроме того, местная инфраструктура здравоохранения тесно связана с государством», - отмечает она. Компании, которые решили остаться, подчеркнули необходимость сохранения доступности жизненно важных препаратов для российских пациентов-участников КИ. Другая причина состоит в том, что остановка в России может потенциально задержать прогресс клинических исследований в целом.
Клинические исследования в России: мало деталей
Хотя ТОП-10 компаний обозначили позицию по клиническим исследованиям в России стратегически, конкретики пока немного. А понимание, какие именно исследования с участием России останавливаются или, вероятно, остановятся в ближайшем будущем, является жизненно важным для индустрии клинических испытаний в целом.
«Когда речь идёт об отмене участия российских клинических центров в международном многоцентровом исследовании, производитель может компенсировать потерю пациентов-участников из России за счёт усиления их набора в других странах», -говорит Недзельска. Бигфарме, возможно, придётся принять решение об открытии новых исследовательских площадок в странах, которые уже участвуют в исследовании или даже о расширении стран. Все эти решения в итоге приведут к ответу на главный вопрос: как не задержать выход на рынок новых лекарств или расширение показаний для уже одобренных препаратов.
Существует также угроза эффекта домино на другие клинические исследования, поскольку рост числа исследований, которые набирают участников в одних и тех же странах, может означать, что компаниям придётся конкурировать за одних и тех же пациентов. Важная причина проведения клинических испытаний в РФ заключается в численности населения. Россия – большая страна с большим количеством потенциальных участников КИ, и восполнить такое количество выбывших из исследований пациентов в других странах может быть непросто.
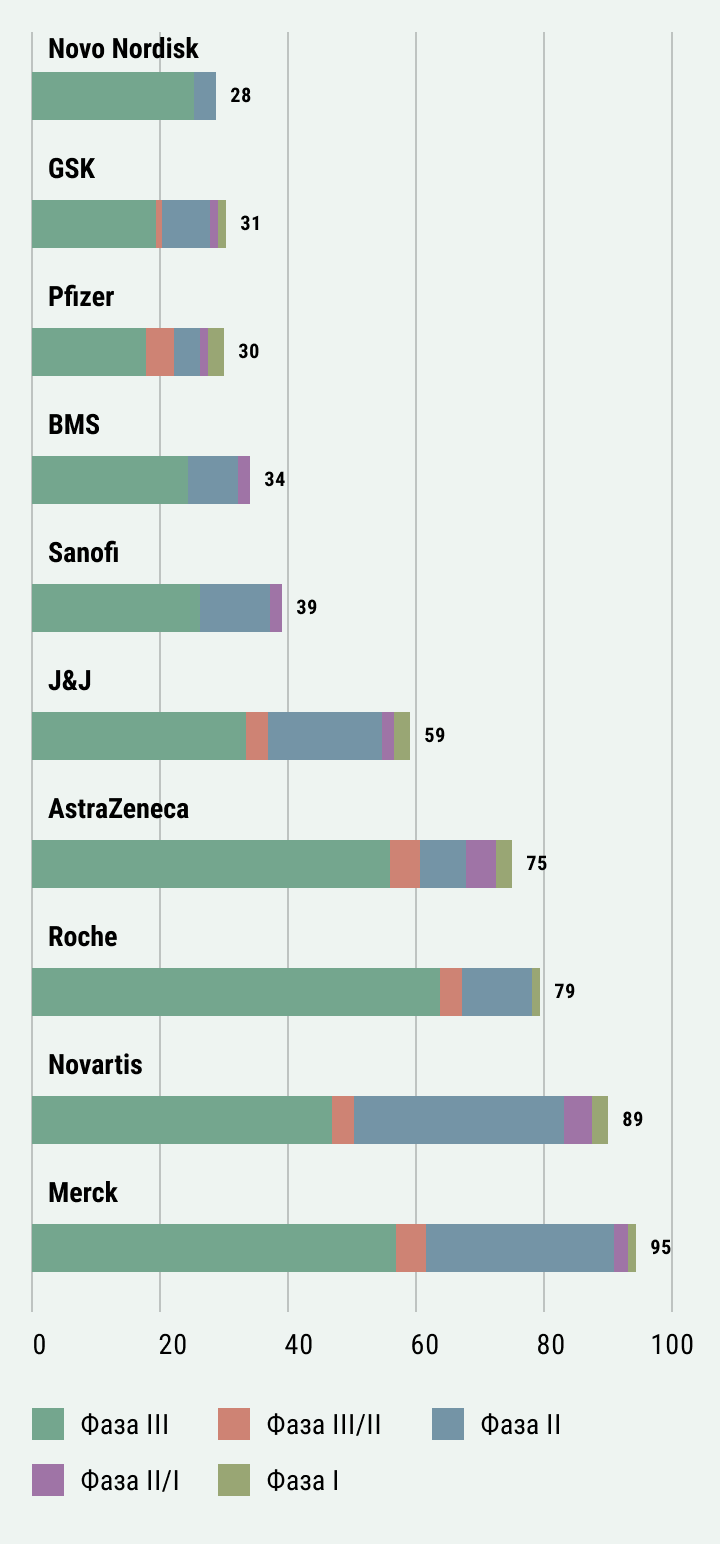
Подавляющее большинство КИ, спонсируемых крупными фармацевтическими компаниями с исследовательскими площадками в России, находятся в фазе III и являются международными и многоцентровыми. Наибольшее количество клинических испытаний III фазы с участием России проводит Roche (64 из 79 испытаний), за ней следуют Merck (59 из 95) и AstraZeneca (54 из 75).
Большинство
клинических исследований фазы I–III, спонсируемых крупными фармацевтическими
компаниями с площадками в России, находятся в фазе III.
Гораздо меньше число локальных КИ, изначально предполагающих набор участников только в России, и все они в настоящее время находятся на запланированной стадии. Novartis проводит пять из таких испытаний: исследование фазы III при системной красной волчанке, исследование фазы II в профилактике болезни трансплантата против хозяина у пациентов с раком крови, фаза II при лёгочной артериальной гипертензии и два исследования фазы I, изучающие сердечно-сосудистые заболевания. Roche проводит исследование гемофилии фазы III A, J & J - исследование бутамирата цитата фазы I, с включением здоровых участников, а GSK - исследование сотровимаба фазы II против Covid-19.
«Для любого исследования, изначально разработанного для рекрутинга участников исключительно в России, где к настоящему времени набор пациентов ещё не начался, наиболее простым выходом может быть его полный перенос в другую страну», -отмечает Недзельска.
Онкология – основная область КИ с участием российских пациентов
Ещё один вывод из анализа материалов бигфармы:
проводимые клинические исследования с участием российских центров преимущественно
специализируются в онкологии -в общей сложности 288 исследования. С большим отрывом от них идут испытания
препаратов для лечения заболеваний центральной нервной системы и инфекционных заболеваний
-36 и 34 соответственно.
Значительное
количество клинических исследований фазы I–III, спонсируемых крупными
фармкомпаниями с площадками в России, приходится на онкологию.

До сих пор лишь несколько КИ полностью остановлены
В то время как компании объявили о своём выходе из России, а также Украины и Беларуси, только несколько клинических исследований были официально отмечены отраслевыми спонсорами как затронутые конфликтом. В частности, пять КИ объявлены как нарушенные и ещё шесть - потенциально нарушенные.
Из всех нарушенных КИ все, кроме одного,
находятся в фазе III. Для шести потенциально нарушенных испытаний три
исследования ФАЗЫ III спонсируются Intra-Cellular Therapies, исследующими
луматеперона тозилат при большом депрессивном расстройстве, и только одно из
этих испытаний принадлежит крупной фармацевтической компании: AstraZeneca Фаза
II AZD1402 при астме.
Исследования фазы I-III, которые были нарушены из-за сложившейся ситуации
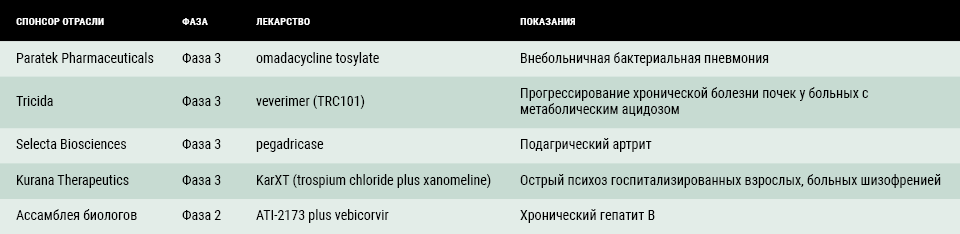
Исследования фазы I-III, в которых отмечались
возможные сбои





