Кто платит за лечение
Кому выгодно?
Компании фармацевтической отрасли стремятся заработать деньги – в этом состоит экономический смысл предпринимательской деятельности, и фарма не исключение. Но в отличие от любой другой индустрии, фармацевтическая работает в области охраны здоровья. Этический конфликт между гуманистической задачей избавления от болезней и извлечением прибыли всегда сопровождал фармацевтических производителей и находился в центре общественного внимания.
Фарма – сложный бизнес, и никому из её игроков не следует забывать: на первом месте всегда стоят интересы пациента. Именно ради лечения и профилактики болезней, ради уменьшения страданий, которые можно предотвратить, крутятся шестеренки всей этой огромной махины. Как выразился в 1950 году, в эпоху зарождения современной фарминдустрии, Джордж Мерк, президент фармгиганта Merck&Co: «мы стараемся никогда не забывать, что лекарства – для людей. Они не для прибыли. Если мы не будем об этом забывать, прибыли не заставят себя ждать. И чем лучше мы будем об этом помнить, тем больше они будут».
Конечно, в фарме, как и в любой индустрии и вообще человеческой деятельности встречаются случаи злоупотреблений, коррупции, сокрытия информации и откровенной лжи. Однако, во всех развитых странах общественный контроль и судебная система в конце концов приводят к разоблачению и наказанию виновных, поэтому таких случаев становится всё меньше.
В итоге можно констатировать, что в мире постепенно складывается экосистема разработки лекарств (она описана в статье «Что такое фарма»), которая позволяет совместить интересы всех игроков: в первую очередь, пациентов и производителей.
Откуда деньги?
Системы здравоохранения большинства развитых стран устроены так, чтобы пациенту (в идеале) не приходилось платить слишком много из своего кармана. Для этого существует страхование. В каждой стране оно устроено по-своему: от всеобщего (впрочем, не без доплат из кармана пациента) государственного страхования, как в России, Германии (там его внедрение началось еще в 1883 году), Франции или Великобритании до полностью частного, как в Нидерландах. Идеальной системы нет нигде: во многих странах людям приходится доплачивать за лекарства из кармана. Например, в России всеобщее лекарственное обеспечение отсутствует. В соответствии с Программой государственных гарантий, медицинская помощь, включая лекарственные средства, оказывается бесплатной только в стационаре. Право на получение лекарственных средств за счёт государства амбулаторно имеют лишь отдельные (льготные) категории граждан. Важный и при этом довольно странный гибрид – в США, представляющий собой лоскутное одеяло из государственных и частных страховщиков и оставляющий миллионы человек вообще без страховки. Затраты США на здравоохранение – самые высокие в мире, и составляют 18% ВВП, при этом эффективность американской системы оставляет желать лучшего.
Тем не менее, именно в США регистрируется больше всего новых лекарств, там же проводится большинство исследований инновационных препаратов. За период с 2011 по 2020 год 43% новых лекарственных препаратов были разработаны на территории США. (по данным Cortellis Compeptitive Intelligence ™). Именно поэтому мы подробнее поговорим о США.
Отчасти дело в том, что в США стоимость новых лекарств не ограничивается законодательно. В ЕС и в России применяются различные способы определения предельной цены лекарств, а в США – это результат непрозрачных переговоров между частными компаниями: производителями лекарств, аптеками и страховщиками. С одной стороны, такая система приводит к самым высоким ценам на лекарства и постоянному их росту. С другой – дает возможность разработчикам лекарств рискнуть, ведь и награда будет велика. Критики этой системы говорят, что необходимо ограничить цены на лекарства в США тем или иным способом, потому что страхование устроено так, что многие люди должны доплачивать за лекарства из собственного кармана. В случае дорогих лекарств это приводит к невозможности оплатить лечение вплоть до полного разорения пациентов. Кроме того, по мнению критиков, несправедливо, что США фактически оплачивают из своего кармана фармацевтические инновации – то есть разработку новых лекарств для всего мира.
По мнению некоторых специалистов, если ограничить стоимость лекарств в США законодательно, это снизит привлекательность сектора биофармацевтики для инвесторов, и новые лекарства будут разрабатываться в гораздо меньшем количестве. Даже если лекарства выходят на рынок по премиальным ценам (а стоимость новых препаратов может составлять сотни тысяч долларов и даже доходить в отдельных случаях до миллионов, как для Золгенсма), через 10-15 лет их ожидает падение цен. Дело в том, что когда действие патента на оригинальное лекарство заканчивается, любой производитель может вывести на рынок копию (воспроизведённый препарат – дженерик для низкомолекулярных веществ или биовоспроизведенный – биоаналог для биопрепаратов), обычно на порядок дешевле оригинала. Фактически, дженериковые лекарства становятся общественным достоянием.
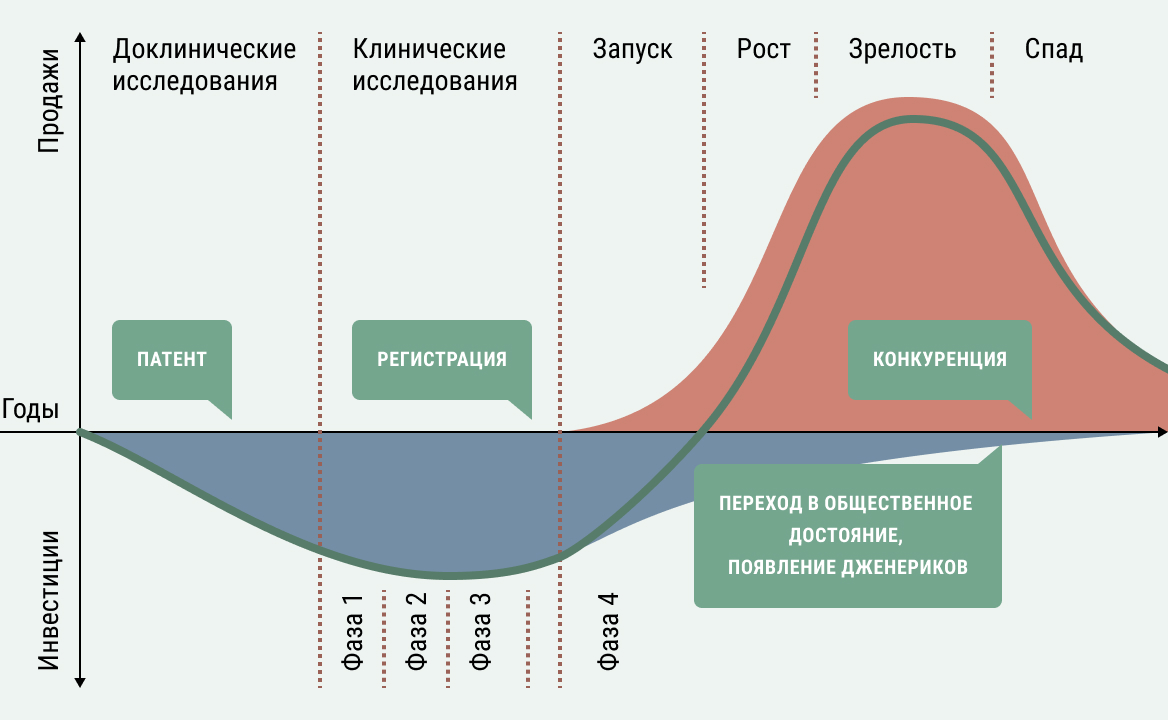
Рисунок 1. Иллюстрация того, как лекарства, выходящие на рынок, сначала растут в цене, а затем резко дешевеют, пополняя арсенал дженериков. Источник
К тому же в США только 15% затрат здравоохранения (в России – 12%) приходится на лекарства (а из них только часть – на новые дорогие препараты). Остальное – это госпитали, оборудование, зарплаты врачам и другие расходы, которые со временем не снижаются в цене, как лекарства, а только растут. Но фармкомпании представляют собой удобную политическую мишень, поэтому их и выставляют крайними.
Старое и новое
Лекарственный рынок очень неоднороден: большинство лекарств, с которыми мы сталкиваемся в повседневной жизни, относительно недороги и существуют на рынке уже десятки лет. Они давно перешли в категорию дженериков – их может выпускать любое фармацевтическое предприятие, потому что патентная защита на них истекла. Цена зависит от рыночных законов, то есть механизмы ценообразования для дженериков такие же, как у любого другого массового продукта.
Другое дело – новые оригинальные препараты: они, как правило, стоят очень дорого и чаще всего относятся к рецептурным специализированным препаратам для лечения тяжелых болезней. Среди них особая, самая дорогая категория – препараты для лечения орфанных (редких) заболеваний. Пациентов, болеющих каждым отдельным заболеванием, мало – порой несколько тысяч на весь мир (хотя суммарно редкими заболеваниями болеет 5% населения Земли). Если новые лекарства для них будут стоить дёшево, компаниям не будет никакого смысла их разрабатывать, потому что это очень рискованное и дорогое дело (подробнее – в статье «Как разрабатывают лекарства»). Однако оказывается, что, несмотря на высокую стоимость новых лекарств, их применение во многих случаях оправдано экономически – об этом ниже. Здесь же заметим, что разработка лекарств, облегчающих страдания людей и спасающих жизни, и есть главная заслуга фармкомпаний, смысл их существования для общества.
Новые препараты пользуются правом патентной защиты, то есть рыночной эксклюзивностью, которая обычно длится лет десять после выхода препарата на рынок. Этот срок – разумный компромисс между желанием компании заработать за счет монопольного положения на рынке и необходимостью снизить цену на препарат, чтобы он стал доступнее для системы здравоохранения. Если бы патентной защиты не было, фирмы, которые не тратили ни копейки на рискованную разработку, могли бы сразу скопировать новый препарат и получать прибыли с его продаж, отнимая их у компании, которая его придумала. Это настолько бы снизило привлекательность новых разработок, что они, скорее всего, практически остановились бы, и общество лишилось бы многих лекарств, способных изменить ход заболеваний. С другой стороны, окончание патентной защиты означает возможность пополнить общественный арсенал медикаментов, о котором идет речь на рис. 1.
Почему так дорого?
Новые лекарства действительно бывают очень дорогими. Чем же обуславливается эта стоимость? Мы уже упомянули, что компаниям необходимо «отбивать» расходы на разработку лекарств – и это правда. В отличие от широко распространенного мифа, фармсектор не прибыльнее других видов легального бизнеса. Фармгиганты тратят миллиарды долларов на разработки новых лекарств: покупая маленькие компании, проводя клинические исследования, строя производственные площадки. Бюджеты на исследования и разработки сравнимы с бюджетами на дистрибуцию и маркетинг, а иногда и превосходят их. Поэтому новые лекарства продаются значительно дороже себестоимости.
Но всё же – как рассчитывается «справедливая» стоимость лекарства? Этим вопросом занимается специальная область знаний – фармакоэкономика. Это подраздел экономики здравоохранения, который позволяет сравнивать ценность лекарств между собой и определять, насколько внедрение нового лекарства влияет на экономические параметры здравоохранения. В рамках фармакоэкономического анализа затраты на лекарство (а также все сопутствующие затраты: на госпитализацию, медперсонал, расходные материалы и т.д.) сопоставляются с эффективностью, безопасностью и пользой, которую приносит лекарство. Как измерить пользу лекарства? Чтобы привести разнообразные исходы лечения в конкретном терапевтическом направлении к единому знаменателю, используют различные методы оценки технологии здравоохранения (ОТЗ). Например, анализ «затраты-эффективность», «затраты-полезность», анализ влияния на бюджет и другие. При проведении оценки используют такие критерии как общая выживаемость, отношение рисков, DALY, QALY и т.д. Давайте рассмотрим для примера, как рассчитывается один из таких показателей при проведении анализа «затраты-полезность» -QALY - quality-adjusted life-year или количество лет жизни с поправкой на её качество (рис. 2).
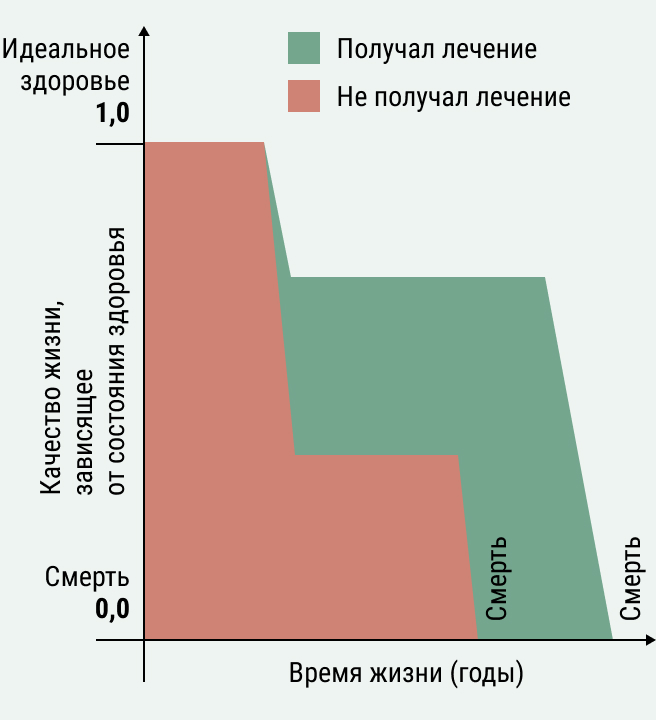
Рисунок 2. Расчет QALY для двух пациентов. По оси Х отложены годы жизни, а по оси Y – качество жизни в условных единицах от 0 до 1. Пациент А не получал новое лекарство и прожил меньше времени с худшим качеством жизни, пациент В – получал новое лекарство и прожил дольше с более высоким качеством жизни. Количество QALY рассчитывается как площадь по кривой зависимости качества жизни от количества прожитых лет.Источник
Можно ли за прибавку одного года жизни со стопроцентным качеством заплатить сто тысяч долларов? А миллион? А миллиард? Сложный этический вопрос. К сожалению, бюджеты здравоохранений не резиновые, и государствам приходится ограничивать затраты на пациента для того, чтобы повысит доступность медицинской помощи для общества в целом.
Интересным примером является подход Великобритании, где давно действует фармакоэкономический орган NICЕ – регулятор, одним из первых внедривший прогрессивные подходы ОТЗ. NICE установил порог в 20-30 тысяч фунтов стерлингов за один QALY. Расчеты NICE являются обязательными для системы государственного страхования в Великобритании, и если показатель превышает пороговую стоимость, скорее всего, новое лекарство не будет одобрено системой страхования (при этом Минздрав Великобритании может одобрить его применение, но пациентам придется платить за него самим). Однако при таком расчёте получается, что некоторые лекарства могут стоить довольно дорого и всё равно покрываться государственной страховкой. Так, если лекарство для лечения редкого заболевания начать давать ребёнку в раннем возрасте, можно увеличить ожидаемый срок жизни и на 20 лет, причём с неплохим качеством. Тогда стоимость в сотни тысяч долларов становится экономически оправданной.
Описанная модель называется value-based pricing (VBP), то есть ценообразование, основанное на ценности (имеется в виду ценность как полезность лекарств или медицинских вмешательств).Однако во многих странах всё ещё используется механизм референсных цен на лекарства, когда цена ограничивается законодательно в зависимости от того, сколько такой препарат стоит в других странах. Внедрение VBP вместо референсного ценообразования в Германии или Швеции, позволило значительно снизить затраты на здравоохранение. А главное – оно даёт фармкомпаниям стимул разрабатывать такие лекарства, которые действительно прибавляют пользы пациентам, а не только немного улучшают существующее лечение, и при этом стоят заоблачных денег просто за новизну.
В России государственное регулирование цен распространяется на лекарственные препараты перечня ЖНВЛП. Для них действует система референтного ценообразования, когда регистрируемая цена референтных лекарственных препаратов не может превышать минимальную цену продаж этого препарата в референтных странах. В последнее время активно внедряются современные подходы к оценке ОТЗ для гармонизации стандартов ОТЗ с европейской практикой.
Бесценный инструмент для фармакоэкономического анализа – сбор данных об эффективности лекарственных средств в реальной клинической практике и их влиянии на исходы здравоохранения. Фармкомпании играют тут важную роль и активно продвигают новые способы сбора и анализа данных, полученных из медицинских карт, носимых устройств с использованием технологий больших данных и искусственного интеллекта. Как рассказывается в статье «Что такое фарма», так фармкомпании становятся не только активными участниками экосистемы разработки лекарств и здравоохранения, но и решительным образом формируют этот ландшафт.




